葡萄糖与氢氧化铜,葡萄糖和氢氧化铜反应化学式

1、葡萄糖和氢氧化铜反应化学式
CH2OH(CHOH)4CHO(葡萄糖) + 2Cu(OH)2(氢氧化铜)=====CH2OH(CHOH)4COOH(葡萄糖酸)+Cu2O(氧化亚铜)+2H2O(水)
若不加热,葡萄糖中含多个羟基,多羟基都可以与Cu(OH)2悬浊液反应,形成绛蓝色溶液,乙二醇、丙三醇等都可以,主要是形成了配合物。
但加热后,就能发生醛基的反应,生成Cu2O红色沉淀了。
化学反应的本质是旧化学键断裂和新化学键形成的过程。
在反应中常伴有发光、发热、变色、生成沉淀物等。判断一个反应是否为化学反应的依据是反应是否生成新的物质。根据化学键理论,又可根据一个变化过程中是否有旧键的断裂和新键的生成来判断其是否为化学反应。
按反应物与生成物的类型分四类:化合反应、分解反应、置换反应、复分解反应。
:百度百科-化学反应
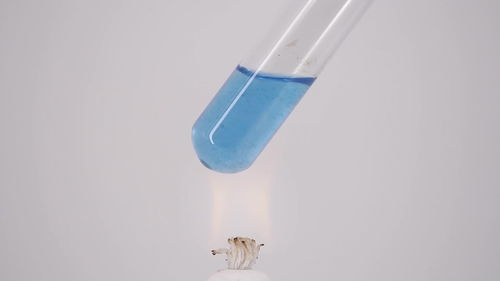
2、氢氧化铜与葡萄糖反应
氢氧化铜(Cu(OH)2)与葡萄糖(C6H12O6)之间的反应实际上是一种氧化还原反应,涉及到氧化剂和还原剂的相互作用。下面详细解释这个反应的步骤和反应:
1、反应方程式:
反应的方程式如下所示:C6H12O6 + 2Cu(OH)2 → C6H12O7 + 2Cu(OH)2
2、反应机理:
在这个反应中,葡萄糖(C6H12O6)是还原剂,而氢氧化铜(Cu(OH)2)是氧化剂。反应的基本机理如下:葡萄糖(C6H12O6)中的一部分碳原子被氧化剂氢氧化铜(Cu(OH)2)的氧氧化成了碳酸(C6H12O7)。
同时,氢氧化铜(Cu(OH)2)中的铜离子(Cu2+)被还原成了铜金属(Cu),从氢氧化铜中析出。
3、反应过程:
在实验中,通常将氢氧化铜的粉末或溶液与葡萄糖的溶液混合。当这两种物质接触时,氢氧化铜的氧氧化葡萄糖的一部分碳原子,同时自身被还原。
反应会伴随着一些观察到的变化,例如反应液可能会变色(因为铜离子还原为铜金属),同时产生的葡萄糖酸可能会增加液体的酸性。
最终,氢氧化铜中的铜金属会在反应中析出,可以通过过滤等方法分离出来。
进行实验时一些重要事项和注意点:
1、阅读实验步骤:
在开始实验之前,仔细阅读实验步骤和材料清单。确保你理解实验的目的、过程和预期的结果。
2、穿戴适当的实验室装备:
穿戴实验室外套、护目镜、手套等防护装备,以防止化学品溅到皮肤或眼睛。确保实验室外套是长袖的,以保护手臂。同时,穿戴封闭式鞋子,以防化学品溅到脚上。
3、操作区域:
在实验室内保持操作区域整洁,避免混乱和拥挤。在实验室内工作时,要将个人物品放置在指定的地方,不要妨碍实验操作。
严格按照实验步骤中的化学品用量和处理方法操作。不要将化学品直接闻、尝、或将手指放入嘴巴,以防止中毒。使用标有化学品名称和危险性的标签的容器,并确保它们密封良好。
4、通风:
在实验室中确保良好的通风,尤其是处理挥发性或有害气体的情况下。如果实验室没有足够的通风,考虑佩戴呼吸面罩或使用化学品吸气罩。

3、葡萄糖与新制氢氧化铜反应是什么
葡萄糖与新制氢氧化铜反应方程式:CH2OH(CHOH)4CHO+2Cu(OH)2-加热->CH2OH(CHOH)4COOH+Cu2O↓+2H2O。
属于氧化反应。葡萄糖溶液与新制氢氧化铜悬浊液反应生成砖红色沉淀(浓度高时生成黄色沉淀)CH2OH(CHOH)4CHO+2Cu(OH)2---加热→CH2OH(CHOH)4COOH+Cu2O↓+2H2O。
实验原理:
葡萄糖分子中含醛基,具有还原性,可被新制氢氧化铜氧化。
实验操作:在试管里加入2 mL 5%的NaOH溶液,滴入2%的CuSO4溶液5滴,混匀,再加入2mL10%的葡萄糖溶液,加热,观察现象。
实验现象及结论:加热前,看到有蓝色沉淀生成;加热后看到有红色沉淀生成。葡萄糖分子中含醛基,具有还原性,可还原新制氢氧化铜悬浊液,生成砖红色氧化亚铜沉淀。
以上内容参考:百度百科-葡萄糖
4、写出葡萄糖与氢氧化铜反应生成砖红色沉淀的化学反应式
葡萄糖可以和新制的氢氧化铜[Cu(0H)2]加热反应生成砖红色沉淀氧化亚铜(Cu20)。首先,在试管中加入2mLl0%的NaOH溶液和5%的CuSO4溶液4~5
滴;接着立刻向其中加入2mL
lO%葡萄糖溶液;然后在酒精灯上加热至沸就可以看到原来的蓝色沉淀[Cu(OH)2]变成了砖红色(Cu20)

请添加微信号咨询:19071507959
最新更新
推荐阅读
猜你喜欢
关注我们


 留学规划
留学规划  留学考试
留学考试  留学指南
留学指南  留学攻略
留学攻略  留学生活
留学生活  留学信息
留学信息  留学专业
留学专业  留学签证
留学签证  关于我们
关于我们  网站首页
网站首页







